"Кратко о гибридизации атомных орбиталей и ковалентных химических связях" - статья из цикла: "Масло-восковая обработка древесины". Одной из основных характеристик ковалентных химических связей является тип перекрывания орбиталей атомов в молекуле. По характеру перекрывания различают σ(сигма)-связи и π(пи)-связи.
Изучение ковалентных химических связей, как правило, начинается с такого явления, как гибридизация атомных орбиталей. Понятие о гибридизации занимает центрально место в методе валентных связей. Гибридизация - удобная модель, объясняющая электронное строение молекул, видоизменения атомных орбиталей и выравнивание длин химических связей и валентных углов в молекуле.
Гибридизация орбиталей - гипотетический процесс смешения разных s-, p-, d-, f-орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим правилам.
Начнём издалека: рассмотрим атом водорода.
Атом водорода имеет только один положительно заряженный протон и один отрицательно заряженный электрон (неспаренный). В спокойном состоянии атома его единственный электрон занимает самый низкий энергетический уровень – 1s-орбиталь.
1s-орбиталь – это двумерное представление орбитали. В действительности она сферическая, и электрон может находиться в любом месте этой электронной оболочки (электронного облака).
Состояние электронной оболочки при наличии неспаренного электрона является незамкнутым (не устойчивым), поэтому атом водорода стремится захватить электрон у соседнего атома и получить стабильную замкнутую конфигурацию. На рисунке ниже один атом водорода совместно использует электрон с другим атомом водорода, образуя молекулу водорода.
Совместное использование электронов действует так, как если бы каждый атом обладал необходимым ему количеством электронов. Когда атомы совместно используют электроны и достигают замкнутой электронной оболочки, то это удерживает их вместе. Их атомные орбитали объединяются, формируя связывающую молекулярную орбиталь вдоль оси, соединяющей ядра.
Такой тип химической связи называется ковалентной σ-связью (сигма-связь). В шаростержневой модели молекулы водорода σ-связь изображена в виде стержня. Стержень имитирует одиночную связь (два спаренных электрона):
Сигма-связь – это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов. Это основная связь в молекуле, которая преимущественно образуется между атомами, она является наиболее прочным типом ковалентной химической связи. Между двумя атомами возможно существование только одной σ-связи.
Когда речь заходит о высыхающих способностях масел и их свойствах, то приходится сталкиваться с понятием двойной связи между атомами, как основной причиной, по которой вообще возможна полимеризация.
Атом водорода не имеет возможности создать двойную связь с другими атомами. Но она вполне реализуется между атомами углерода, который в возбуждённом состоянии имеет четыре неспаренных электрона и может участвовать в образовании четырёх ковалентных связей.
При количестве электронов в атоме более двух, число орбиталей увеличивается, а форма их становится более разнообразной.
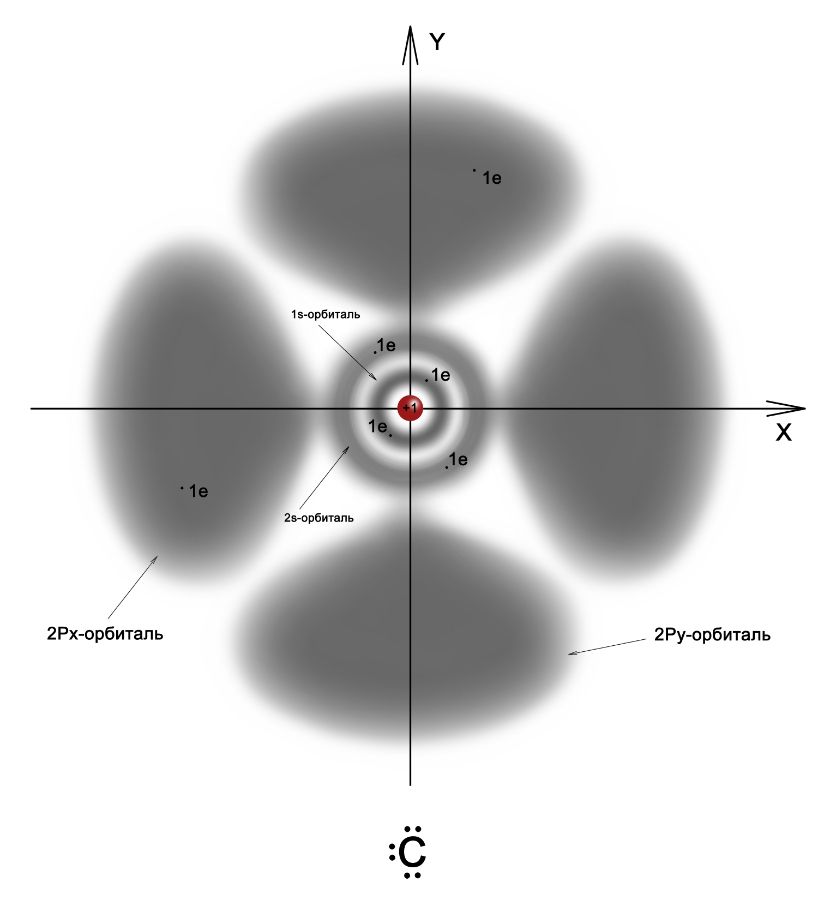
Электроны заполняют орбитали по строго определённым правилам. После заполнения сферической 1s-орбитали, заполняется сферическая 2s-орбиталь. Следом за 2s-орбиталью электроны распределяются на 2p-орбиталях, имеющие уже не сферическую, а гантелеобразную форму (или форму объёмной восьмёрки). 2p-орбиталей у атомов – три, ориентированных по осям X, Y, Z. На рисунке ниже 2pZ-орбиталь (не показана) располагается перпендикулярно плоскости экрана.
Орбитали, изображённые на схеме считаются НЕгибридными. Они характерны для атомов, находящихся в своём обычном спокойном состоянии. В возбуждённом состоянии происходит выравнивание электронной плотности атомных орбиталей разного типа с образованием новых молекулярных орбиталей, форма и энергия которых одинаковы. Это выравнивание называется гибридизацией атомных орбиталей.
В гибридизацию вступают атомные орбитали с небольшой разницей в энергии, то есть, близких энергетических уровней, например, 2s и 2p.
Так, в возбужденном атоме углерода, один спаренный электрон, находящийся на 2s-орбитали переходит на свободную 2pZ-орбиталь. В результате атом углерода получает 4 неспаренных электрона (один электрон на 2s-орбитали и по одному электрону на орбиталях 2pX, 2pY, 2pZ) и, соответственно, способность образовывать 4 ковалентные связи.
Форма гибридных орбиталей становится одинаковой, а их количество определяется числом исходных орбиталей, участвующих в таком «смешении». Выделяется три основных вида гибридизации: sp, sp2, sp3.
Для sp-гибридизации характерно «смешение» 2s-орбитали с одной 2p-орбиталью. Другие две 2p-орбитали в гибридизации не участвуют и остаются НЕгибридизованными.
SP-гибридизация приводит к следующему строению атома углерода: по оси X располагаются две гибридизованные sp-орбитали, на оси Y остаётся НЕгибридизованная 2pY-орбиталь, на оси Z (перпендикулярно плоскости экрана) также остаётся НЕгибридизованная 2pZ-орбиталь (на рисунке не показана).
Атомы, находящиеся в sp-гибридизации, соединяясь друг с другом, образуют молекулы линейной формы.
Для sp2-гибридизации характерно «смешение» одной 2s-орбитали с двумя 2p-орбиталями. Третья 2p-орбиталь остаётся нетронутой и в гибридизации не участвует. В результате sp2-гибридизации образуется три гибридных 2p-орбитали.
Допустим, что в нашем примере 2s-орбиталь «смешивается» с орбиталями 2pX и 2pZ. Тогда, если посмотреть на результат такого «смешения» сверху на ось Y, то мы будем иметь следующую картину:
Три гибридизованные 2p-орбитали лежат в одной плоскости и образуют равносторонний треугольник. НЕгибридизованная 2pY-орбиталь располагается перпендикулярно им (перпендикулярно плоскости экрана).
Атомы, находящиеся в sp2-гибридизации, соединяясь друг с другом, образуют молекулы плоской двумерной формы.
При взаимодействии двух атомов углерода, находящихся в состоянии sp2-гибридизации, между ними образуются две связи. Первая связь возникает между двумя взаимно перекрывающимися гибридными 2p-орбиталями. В этом случае мы имеем знакомую нам σ-связь. Вторая связь образуется при перекрытии двух НЕгибридизованных 2pY-орбиталей в плоскости, перпендикулярной оси, соединяющей ядра атомов, «сверху» и «снизу» от неё (боковое перекрывание). Эта связь называется π-связью.
П-связь, как и σ-связь является ковалентным типом химической связи - образуется двумя парами электронов. Она всегда возникает только как дополнительная к σ-связи и не может существовать в отдельности от неё. Если к σ-связи добавляется π-связь, то принято считать, что атомы удерживаются двойной связью. Электроны π-связи более удалены от ядер атомов, поэтому в меньшей степени удерживаются ими. В следствие этого π-связь менее прочная и легче разрывается при химических реакциях. На шаростержневых моделях двойная связь изображается в виде двух стержней:
Первый стержень – это σ-связь, второй стержень – π-связь.
Как можно заметить, σ-связь возникает не только между сферическими s-орбиталями. Она легко образуется при взаимном перекрытии НЕгибридизованных s-, p- и гибридизованных атомных орбиталей. Основной признак, по которому выделяют σ-связь среди прочих – это её расположение на оси, соединяющей ядра атомов.
Ещё раз проговорим: если атомы в молекуле связаны только σ-связями, то эти связи будут считаться одиночными. Если к σ-связи добавляется π-связь, то между атомами возникает двойная связь. Двойная связь состоит из прочной σ-связи и менее прочной π-связи.
В различных источниках эти два типа ковалентной связи часто изображают в виде таких схем:
Жирные точки обозначают ядра атомов, окружности и восьмёрки - s- и p-орбитали соответственно, заштрихованная область - место образования ковалентной химической связи.
SP3-гибридизацию подробно рассматривать не будем. Отметим лишь, что в данном виде гибридизации участвуют все четыре орбитали: 2s, 2pX, 2pY и 2pZ. При их "смешении" возникают четыре гибридные орбитали, которые расходятся к вершинам правильного тетраэдра. Атомы, находящиеся в sp3-гибридизации образуют пространственные формы молекул.
При sp-гибридизации между атомами, как правило, возникает тройная связь (одна σ-связь и две π-связи), при sp2-гибридизации - двойная (одна σ-связь и одна π-связь), при sp3-гибридизации атомы имеют только одиночные σ-связи.
В дальнейшем, когда нам встретится такое понятие, как двойная связь в молекуле, например, олеиновой, линолевой и других кислот, входящих в состав высыхающих масел, мы будем знать, что она означает, и как устроена.